Micro ARN: llave maestra en la fisiopatología cardíaca
Los micro ARN (miARN, ácidos ribonucleicos monocatenarios) son un nuevo tipo de genes con una longitud entre 21 y 23 nucleótidos. Poseen la capacidad de regular la expresión génica, por lo tanto son jugadores claves en muchos procesos fisiológicos, de desarrollo y en una gran cantidad de enfermedades humanas, incluyendo el cáncer. Los miARN son secuencias de ARN transcritas a partir de ADN, pero no se traducen en proteínas. La secuencia de ADN que codifica para un miARN tiene una extensión que supera al tamaño final del propio miARN e incluye la región miARN y una zona complementaria a la anterior, lo que permite su apareamiento. Esto conlleva a que la transcripción de esta secuencia de ADN se formen regiones que tienen la capacidad de generar una horquilla y constitur ARN bicatenario. La función de los miARN está relacionada con la regulación de la expresión génica, de esta forma un miARN es complementario a una parte de uno o más ARN mensajeros (ARNm). Los miARN de animales suelen complementar con la región 3' UTR, mientras que los de plantas generalmente complementan con regiones codificantes. El apareamiento del miARN con el ARNm inhibe su traducción a proteína y facilita su rotura.
Los miARN, que se descubrieron hace más de una década, se han convertido rápidamente en un foco importantísimo de estudio científico. Lamentablemente, los roles reguladores de estos minúsculos ARN siguen siendo misteriosos ya que los investigadores sólo han podido determinar la función de poco más de 200 conocidos. A diferencia de las moléculas más grandes de ARN mensajero que llevan información genética desde los genes hasta la maquinaria de producción de proteínas, los miARN regulan la actividad génica al interferir con el mensaje genético que se encuentra en las moléculas mensajeras.
Por otra parte, las enfermedades cardiovasculares representan la causa más frecuente de morbilidad y mortalidad en el mundo industrializado. Aunque se ha avanzado enormemente en entender la patogénesis molecular del corazón, falta mucho por descubrir y poder crear nuevas oportunidades terapéuticas. Es esencial descifrar los caminos moleculares y las alteraciones asociadas que conducen a las anormalidades del corazón adulto. La remodelación morfológica que incluye importantes cambios estructurales tales como la fibrosis intersticial y la hipertrofia del cardiomiocito, es un importante determinante de enfermedades cardíacas. La inhibición de la traducción y/o la degradación de los mensajeros “blanco” de ARN es un mecanismo frecuente de la acción de los miARNs. Éstos realizan funciones importantes durante el desarrollo embrionario cardiaco. Además, recientemente han sido implicados en la hipertrofia y en la insuficiencia cardiaca, pero su posible papel en la remodelación estructural y eléctrica del corazón durante el envejecimiento no se ha dilucidado todavía.
Los Micro ARN y la insuficiencia cardíaca
Intensa ha sido la búsqueda de los mecanismos básicos responsables del desarrollo y progresión de la insuficiencia cardíaca. A pesar del descubrimiento de una variada gama de procesos relevantes en la traducción de señales que pueden provocar el avance de la enfermedad (por ejemplo, las que activan la angiotensina y las vías adrenérgicas), los medios por los cuales estos caminos son coordinados con respecto al desarrollo y a la progresión de la insuficiencia cardíaca siguen siendo poco claros. Un reciente estudio de Van Rooij y colegas (Science 2007; 316:575-9) es particularmente interesante porque proporciona una nueva comprensión de cómo se coordinan las respuestas al estrés en el corazón enfermo.
El corazón responde al daño o a la sobrecarga hemodinámica activando una variedad de señales intracelulares y mediadores transcripcionales que da lugar a un supuesto fenotipo que consiste en la hipertrofia del miocito, la re-expresión de un patrón génico embrionario (incluyendo la estimulación de genes fetales estructurales, como el de la cadena pesada de la beta miosina, y la inhibición de los genes estructurales adultos, por ejemplo el de la cadena pesada de la alfa miosina), y la remodelación de la matriz extracelular. Estos acontecimientos conducen a la dilatación ventricular izquierda (remodelación) y a la fibrosis progresiva del miocardio.
El grupo de Van Rooij había descrito previamente un patrón de expresión de micro ARN (miARN) asociado a la hipertrofia y al paro cardíaco en ratones y en seres humanos. El miARN es un pequeño ARN que no codifica proteínas, sin embargo, interactúa con ARN mensajeros (los ARNm) de una manera secuencia-específica regulando negativamente la expresión de los ARNm por degradación o directamente inhibiendo su traducción (Figura 1). Aunque los miARN comúnmente inhiben la expresión de los genes, también pueden provocar una sobre regulación génica de forma negativa al modular la expresión de genes inhibitorios. Alternativamente, la regulación negativa de los miARN también puede conducir a la reactivación de los genes que se han suprimido previamente.
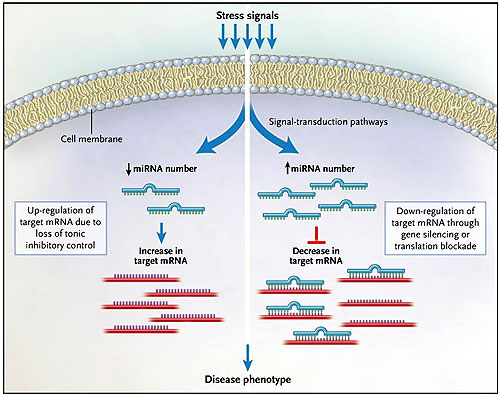
Las señales de estrés (como la sobrecarga hemodinámica) activan las vías de transducción que conducen al aumento o a la disminución de micro ARN específicos (miARN). El estrés provoca el incremento de los miARN cuando a su vez disminuyen algunos tipos de ARN mensajeros (ARNm) a través del bloqueo de un gen o el bloqueo de la traducción del ARNm respectivo. Inversamente, el estrés puede inhibir un miARN dando lugar al incremento de los ARNm debido a la pérdida del control inhibitorio tónico del miRNA sobre su ARNm respectivo. En última instancia, es el cambio en la expresión génica lo que contribuye al fenotipo resultante de la enfermedad. Van Rooij y colaboradores demostraron recientemente que la ausencia de un ARNm específico previene la hipertrofia cardiaca y potencia la producción de la cadena pesada de la beta miosina después de una sobrecarga hemodinámica, indicando que este miARN es crítico en el desarrollo de la insuficiencia cardíaca.
Van Rooij y colaboradores demostraron que la sobre expresión de miARN inducidos individualmente era suficiente para generar un crecimiento hipertrófico de los miocitos cardiacos aislados y provocar una cardiomiopatía dilatada en ratones transgénicos, sugiriendo que la presencia de micro ARN individuales es suficiente para provocar enfermedad cardíaca. En su estudio más reciente, el mismo grupo demostró que la deleción de miR-208, un miARN cardiaco muy específico que codifica para un intrón en el gen de la cadena alfa miosina, protege a los ratones contra la hipertrofia cardiaca del miocito, de la sobre regulación de la cadena pesada de la miosina beta, y de la fibrosis del miocardio en respuesta a la señal tiroidea y a la sobrecarga hemodinámica. También demostraron que los animales mutantes deficientes en miR-208 no potencian la expresión cardiaca de la cadena pesada de la beta miosina en respuesta a la señal tiroidea.
Todas estas observaciones sugieren que miR-208 es un punto nodal específico para cada tipo de tejido capaz de integrar señales de estrés y de coordinar la expresión de genes y proteínas lo que contribuye al desarrollo del fenotipo de la insuficiencia cardiaca. El grupo de Van Rooij se centró en identificar a un inesperado mediador de la remodelación cardiaca que era inducido por la tiroides, el receptor de la hormona tiroidea asociada a la proteína 1 (THRAP1, por sus siglas en inglés), en base a la unión de miR-208 con una región del promotor de THRAP1, una conexión previamente desconocida.
Dada la complejidad de la insuficiencia cardíaca, es difícil pensar que la identificación de miARN específicos para diferentes enfermedades conducirá al reemplazo de las actuales estrategias terapéuticas por nuevos medicamentos o dispositivos en un futuro próximo. Sin embargo, al identificar los micro ARN respectivos para ciertas patologías, los investigadores pueden utilizar algoritmos computacionales para identificar áreas desconocidas dentro de una vía patológica de interés con la finalidad de modificar sitios específicos en los miARN y el subsiguiente manejo de la enfermedad. Esta aproximación podría conducir en última instancia a nuevas estrategias y a acercamientos terapéuticos innovadores en la insuficiencia cardiaca, así como en otras enfermedades, tales como la hipertensión, deterioro muscular y cáncer.
Fuente bibliográfica
MicroRNAs and the Failing Heart
Douglas L. Mann, M.D.
Winters Center for Heart Failure Research, Baylor College of Medicine, Houston, USA.
N Engl J Med. 2007 Jun 21; 356(25):2644-5


