Hormona del corazón contra la grasa
La obesidad está aumentando en todo el mundo. Esto representa un factor de riesgo subyacente de enfermedad cardiovascular y diabetes tipo 2. Los factores de riesgo que predisponen a la diabetes y condiciones cardiovasculares constituyen el síndrome metabólico, condición que se ve incrementada con la edad. La obesidad interfiere con muchas y diferentes vías metabólicas que subyacen a numerosos factores de riesgo.
Por otra parte, en seres humanos normales y obesos, la movilización de lípidos y las concentraciones plasmáticas de ácidos grasos no esterificados están controladas por catecolaminas (por ejemplo, la epinefrina y norepinefrina) y la insulina. Por su parte, los péptidos natriuréticos juegan un papel clave en la regulación del equilibrio de la sal y del agua y la homeostasis de la presión arterial. Ellos están involucrados en la fisiopatología de la hipertensión y la insuficiencia cardíaca. Recientemente se ha determinado que los péptidos natriuréticos también ejercen un potente efecto lipolítico (es decir, la activación de la descomposición de los triglicéridos almacenados) en células grasas aisladas y promueven la movilización lipídica in vivo. En consecuencia, es necesario dilucidar los mecanismos moleculares de acción de los péptidos natriuréticos y su contribución al control fisiológico de la movilización de lípidos.
Los péptidos natriuréticos y metabolismo de la grasa
La íntima conexión entre los trastornos metabólicos y el riesgo cardiovascular está realzada por el enfoque de las "enfermedades cardiometabólicas" en las guías de práctica clínica y la literatura biomédica. El conocimiento convencional sugiere que la causalidad fluye en una dirección: enfermedades metabólicas como la obesidad o la resistencia a la insulina desencadenan anormalidades cardiovasculares. Sin embargo, hay un reconocimiento creciente que el corazón no es sólo un espectador pasivo en el proceso, ya que puede desempeñar un activo papel contra enfermedades metabólicas, como lo demuestra un reciente estudio realizado por Marica Bordicchia y colaboradores (J Clin Invest 2012; 122:1022-36).
El hecho que el corazón pueda influir en el funcionamiento de otros órganos de manera endocrina se hizo evidente en la década de 1980. El órgano segrega una familia de hormonas conocidas como péptidos natriuréticos, los cuales regulan la natriuresis, diuresis y vasodilatación, que en conjunto sirven para contrarrestar el exceso de estrés de la pared cardíaca. Sin embargo, los receptores de los péptidos natriuréticos no se limitan a los riñones y la vasculatura. Un tejido diana es la grasa, que es rica en receptores que se unen al péptido natriurético auricular y al péptido natriurético tipo B (NPR-A), así como a receptores que promueven su eliminación (NPR-C).
Hasta hace algún tiempo, poco se sabía sobre la importancia del sistema de péptidos natriuréticos en la grasa. Los estudios experimentales les asignan características de reguladores metabólicos: estimulan la lipólisis de una manera similar a la de las catecolaminas, y los ratones que sobre-expresan el péptido natriurético tipo B están protegidos de la ganancia de peso y de la intolerancia a la glucosa cuando son sometidos a dietas ricas en grasas.
El estudio realizado proporciona más evidencia sobre los mecanismos biológicos subyacentes. Los investigadores examinaron ratones modificados genéticamente que carecen de NPR-C. Estos animales mejoraron la señalización del péptido natriurético debido a su disminución en los órganos diana. No sólo se encontró una reducción de la masa grasa en animales knock-out para NPR-C, en comparación con ratones tipo salvaje, sino que también se observó que los genes de los adipocitos marrones se expresaban a niveles elevados. Los adipocitos marrones, a diferencia de los blancos, promueven la utilización de mayor energía y la generación de calor (termogénesis), desplazando el equilibrio metabólico hacia el consumo de calorías. Así, el “pardeamiento” de los adipocitos, en combinación con la lipólisis mejorada, proporciona un mecanismo de peso para un efecto favorable metabólico de los péptidos natriuréticos (fig. 1).
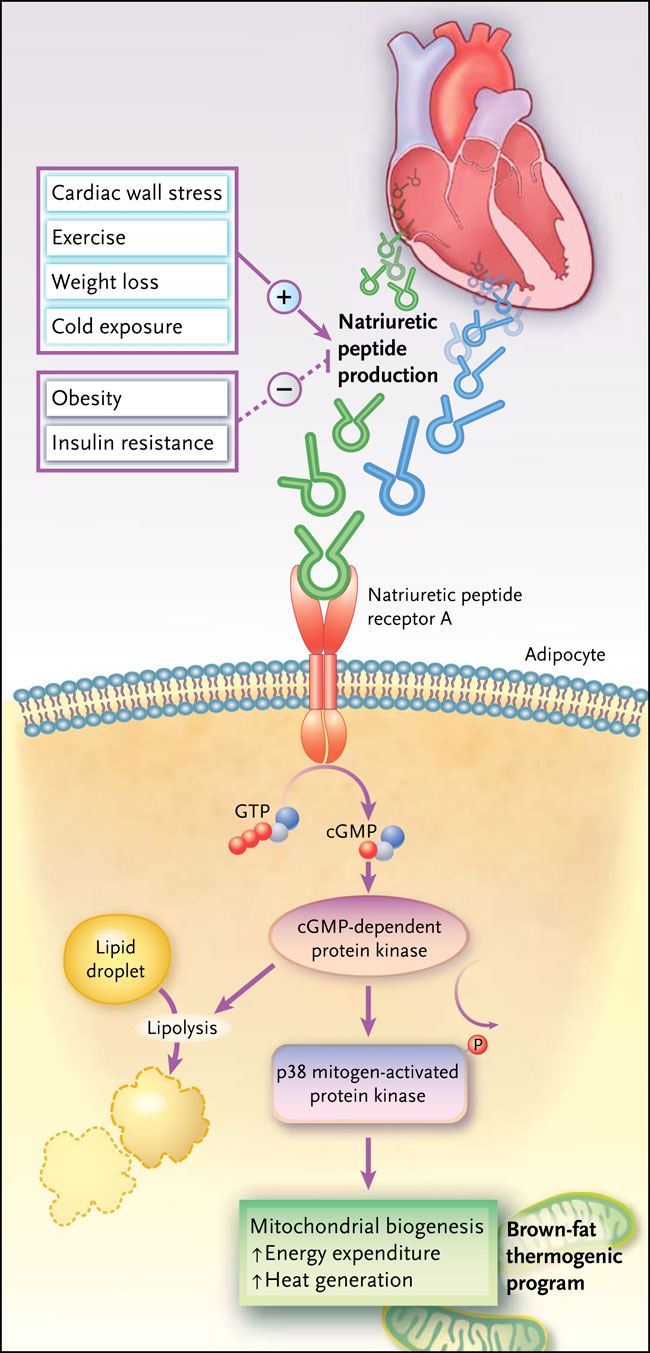
El corazón sintetiza hormonas peptídicas conocidas como péptidos natriuréticos cuya expresión está regulada por el estrés de la pared cardíaca, pérdida de peso, ejercicios y exposición al frío, que a su vez es suprimida por la obesidad y la resistencia a la insulina. Se ha demostrado que estas proteínas son importantes reguladores de los adipocitos. El receptor objetivo para la circulación de péptidos natriuréticos es el receptor del péptido natriurético A (NPR-A), una ciclasa guanilato unida a membrana. La unión de péptidos natriuréticos a NPR-A en los adipocitos conduce a la producción de monofosfato cíclico de guanosina (cGMP). El GMPc activa la proteína quinasa dependiente de GMPc (PKG). La fosforilación mediada por PKG desencadena una cascada que incluye el incremento de la lipólisis y la activación de la proteína quinasa p38, convirtiéndose en el programa termogénico de la grasa parda. GTP denota trifosfato de guanosina.
Los autores confirmaron estos hallazgos en ratones tipo salvaje tratados con infusiones de péptido natriurético, lo que dio lugar a un marcado aumento en la expresión de los genes asociados a los adipocitos marrones en el tejido adiposo, demostrando la activación del tejido adiposo marrón y el “pardeamiento” del tejido adiposo blanco. Los ratones tratados presentaron un mayor consumo de oxígeno y gasto energético, compatible con una gran actividad de los adipocitos marrones. También se realizaron experimentos en dos líneas independientes de células adiposas humanas: células madre adiposas y adipocitos subcutáneos. Al igual que en los modelos animales, la administración del péptido natriurético auricular aumentó significativamente las transcripciones de los genes de los adipocitos marrones, así como los marcadores de la biogénesis mitocondrial y el consumo de oxígeno celular. En el trabajo in vitro estas acciones estuvieron mediadas por dos quinasas específicas (enzimas que participan en la señalización celular) y se sumaron a los efectos de la activación beta-adrenérgica.
Estos nuevos hallazgos amplían la lista de funciones positivas realizadas por los péptidos natriuréticos. También reorientan la atención sobre los factores que influyen en su actividad, que podrían proporcionar la susceptibilidad a enfermedades cardiometabólicas y plantear objetivos para la intervención. Aparte de los elementos desencadenantes hemodinámicos clásicos de la liberación del péptido natriurético, se han descrito una serie de estímulos novedosos, incluyendo la pérdida de peso, ejercicios y la exposición al frío. Estas observaciones plantean la interesante posibilidad que el péptido natriurético pueda quedar atrapado en un círculo vicioso en el cual un sistema de supresión conduzca a un deterioro adicional en la capacidad de resistir a la acumulación de grasa. Es tentador especular que el aumento farmacológico del péptido natriurético pueda ayudar a romper este ciclo. Los efectos lipolíticos y marrones de los péptidos natriuréticos son compartidos por el sistema adrenérgico, pero las intervenciones dirigidas hacia él son más atractivas debido a que podrían evitar los efectos deletéreos de la activación adrenérgica sobre la función cardiovascular. De hecho, las moléculas que son capaces de reducir la presión arterial, evitar la retención de sodio y reducir la acumulación de grasa, son las más ideales para luchar contra las enfermedades cardiometabólicas.
Fuente bibliográfica
The Natriuretic Peptides and Fat Metabolism
Thomas J. Wang, M.D.
Cardiology Division, Massachusetts General Hospital, Boston.
N Engl J Med 2012; 367:377-378