Clonación humana en células madre
Las células madre pluripotentes inducidas (iPSC) representan una oportunidad única para la medicina regenerativa, ya que tienen la posibilidad de producir cantidades ilimitadas de células para el trasplante autólogo, con potencial aplicación en una amplia gama de trastornos. Sin embargo, su uso humano en el contexto de una enfermedad heredada genéticamente requiere de la corrección de mutaciones que podrían se causantes de enfermedades de una manera que sea totalmente compatible con aplicaciones clínicas. Los métodos actualmente disponibles, tales como la recombinación homóloga, carecen de la eficacia necesaria y también dejan secuencias residuales en el genoma intervenido. Por lo tanto, el desarrollo de nuevos enfoques para modificar el genoma de los mamíferos es un requisito previo para cumplir la promesa clínica de las iPSC humanas.
Terapia genética y células madre
Las terapias basadas en células madre tienen el potencial de reparar e incluso corregir los defectos relacionados con enfermedades humanas. Aunque algunas aplicaciones han avanzado en el ámbito clínico, el progreso parece ser lento, y los desafíos éticos todavía no se han abordado completamente. El objetivo del desarrollo de células pluripotentes que puedan transmutar a órganos específicos y maduros, y posiblemente curar muchas patologías humanas, aún no se ha alcanzado.
Con los recientes avances, sin embargo, la corrección de genes con células madre está más cerca de alcanzarse. Aunque las técnicas para la rectificación de anomalías genéticas han estado disponibles en los laboratorios durante años, la manipulación del genoma suele dejar rastros de material genético no deseado al interior de la célula o dentro de los mismos genes. Recientemente, Kosuke Yusa y colegas (Nature 2011; 478:391-4) acaban de describir un estudio que implica la corrección de una sola mutación genética en células madre pluripotentes inducidas (iPSC, por sus siglas en inglés) derivadas de pacientes con fibroblastos dérmicos propios (dado que estas células madre derivan típicamente de una célula somática diferenciada, son distintas de las células madre embrionarias porque derivan de los primeros embriones). Utilizando técnicas que aparentemente no dejan secuencias residuales, estos investigadores sustituyeron una secuencia de ADN mutado en iPSC de pacientes con un gen normal.
Los autores decidieron estudiar la deficiencia de alfa1-antitripsina, que es causada por mutaciones en SERPINA1, el gen que codifica el inhibidor de la proteasa de serina (PI). La variante "normal" (designada PI*M) difiere del más común, siendo genotipo deficiente (PI*Z) por un solo par de bases, dando lugar a la sustitución de un aminoácido (Glu342Lys) en la proteína alfa1-antitripsina. Las iPSC corregidas fueron estimuladas para adquirir las características de los hepatocitos, incluyendo la síntesis y secreción de la alfa1-antitripsina normal. Después de la inyección intraesplénica en ratones, estas iPSC derivadas colonizaron el hígado de los animales y mantuvieron sus características como en los hepatocitos y produjeron la alfa1-antitripsina durante varias semanas.
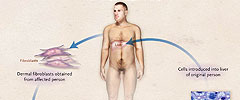
La carencia de alfa1-antitripsina es sólo una de las muchas enfermedades monogénicas que podrían ser objetivos potenciales para este tipo de enfoque correctivo. El grupo de K. Yusa postula que esta tecnología es segura y efectiva, y que las iPSC derivadas de una persona podrían ser reinsertadas - corregidas y parecidas a los hepatocitos - a la misma persona en aproximadamente 4 meses (fig. 1). Aunque es difícil de lograr el doble objetivo de seguridad y eficacia en cualquier nuevo agente terapéutico, el uso de iPSCs manipuladas genéticamente como forma terapéutica plantea problemas específicos de seguridad, algunos de los cuales ya han sido analizados por estos investigadores. Por ejemplo, mediante el uso de células madre nativas (derivadas de las propias células somáticas), se han dado pasos importantes hacia la solución de un posible rechazo o reacción a los hepatocitos derivados de iPSC.

El diagrama representa un modelo de cómo un hombre o mujer con deficiencia de alfa1-antitripsina pueden ser tratados con células madre pluripotentes inducidas (iPSCs) que son corregidas. Si la terapia correctiva se lleva a cabo, los hepatocitos derivados del propio paciente podrían colonizar y tal vez remplazar a las células hepáticas existentes. Como los hepatocitos nativos dañados mueren debido al exceso de proteína alfa1-antitripsina mutante, las unidades anormales podrían ser sustituidas por hepatocitos corregidos.
Las células madre acumulan mutaciones en su genoma, ya que se multiplican en cultivo. Algunas alteraciones son predecibles y bien caracterizadas, mientras que otras parecen ocurrir al azar. Una mutación adquirida podría poseer propiedades oncogénicas y dar lugar a la neoplasia. Los autores ofrecen dos observaciones en relación con estas preocupaciones: ellos compararon las mutaciones adquiridas durante el crecimiento en cultivo de iPSC no corregidas y de iPSC corregidas genéticamente, y no encontraron diferencias importantes entre ambos tipos. También observaron que no existieron tipos de cáncer en aquellos ratones que habían recibido iPSC modificadas. Aunque estos hallazgos son tranquilizadores, sólo representan un primer paso hacia la documentación de seguridad en tales procedimientos.
Suponiendo que finalmente se abordará la seguridad de las iPSC, podríamos especular acerca de la aplicación clínica como terapia específica en la alfa1-antitripsina. La insuficiencia hepática se desarrolla durante los primeros meses de vida en un 2 a 3% de los bebés que nacen con esta deficiencia. El uso de iPSC corregidas para prevenir la enfermedad en los lactantes, probablemente implicaría el tratamiento intrauterino o la manipulación de embriones antes de la implantación (aunque podría ser más fácil seleccionar un embrión que carece de la mutación, si hay uno disponible). Este enfoque se acerca a lo que podría considerarse en las células embrionarias madre, lo que sería más seguro en la persona afectada. La lesión hepática más insidiosa, por lo general manifestada como cirrosis, puede ocurrir en cualquier momento en las personas con deficiencia de alfa1-antitripsina. La enfermedad pulmonar destructiva es la otra manifestación clínica de este trastorno. Se sabe que los factores ambientales aumentan el riesgo de cáncer de pulmón y de enfermedades al hígado en pacientes con este trastorno y que la exposición durante la infancia es al menos tan importante como la exposición en el futuro. Por lo tanto, el enfoque de "iPSC corregidas" puede ser la mejor aplicación durante los primeros años de vida, por lo que en términos de seguridad está mejor posicionado, especialmente en relación con el riesgo de neoplasia.
Fuente bibliográfica
Gene Therapy Meets Stem Cells
Robert A. Sandhaus, M.D., Ph.D.
National Jewish Health, Denver, USA.
N Engl J Med. 2012 Feb 9; 366(6):567-9