Edema retinal, una gota a la vez
La anormal permeabilidad vascular de la retina conduce a edema en la zona de la mácula, siendo la principal causa de pérdida de la visión en enfermedades como la retinopatía diabética, degeneración macular exudativa, oclusiones vasculares retinianas y en condiciones inflamatorias y neoplásicas. Aunque una gran variedad de procesos pueden conducir a un aumento de permeabilidad vascular a través de diferentes mecanismos, la citoquina llamada factor de crecimiento endotelial vascular (FCEV) activa las vías de pérdida vascular. Los niveles del FCEV se correlacionan con una mayor permeabilidad vascular isquémica en las retinopatías y posiblemente también en la degeneración macular exudativa y en la uveitis. De hecho, sus antagonistas se utilizan con éxito para reducir el edema macular/retinal y en enfermedades oculares neovasculares como la degeneración macular senil con una estabilización o incluso mejora de la agudeza visual en subconjuntos de pacientes afectados.
Por su parte, las células del epitelio pigmentario de la retina son las células fagocíticas más activas del cuerpo humano. Son capaces de seleccionar, procesar y metabolizar compuestos esenciales para la función visual como la vitamina A y los ácidos docosahexaenoicos. Además, tienen un rol protagónico a la hora de regular las vías de señalización intercelular, expresión genética, transporte de proteínas, y otras funciones importantísimas, por consiguiente, no es raro que estén involucradas en enfermedades degenerativas de la retina. El FCEV es un mitógeno celular específico endotelial, que está involucrado en la angiogénesis para el crecimiento de tumores sólidos y en enfermedades retinales. Este factor de crecimiento vascular se expresa en la glia y en las células del epitelio pigmentario de la retina.
Por ejemplo, en la evolución temprana de la degeneración macular asociada a la edad neovascular, o DMAE, la combinación de varios factores estimulan la sobre-expresión patológica del FCEV, que es una proteína que sirve como una señal esencial en la causa subyacente de todos los casos de DMAE neovascular y es responsable de estimular la angiogénesis (crecimiento anormal de los vasos sanguíneos) y extravasación de líquidos (salida de la circulación de los tejidos); dos sellos característicos de la DMAE neovascular. Dada su importancia, entonces, el FCEV representa un interesante blanco terapéutico.
La orientación intraocular
Salvo la muerte, la ceguera es una de las complicaciones más temidas de las enfermedades humanas. En los países desarrollados, la pérdida visual resulta principalmente de la neovascularización patológica de la coroides y de la retina o por edema de la retina, condiciones reguladas básicamente por la molécula angiogénica y de vasopermeabilidad: el factor de crecimiento endotelial vascular. Estas complicaciones son tratadas con fotocoagulación mediante láser, que también destruye otras áreas funcionales de la retina, o por agentes antiangiogénicos que se inyectan repetidas veces en el centro del ojo. Recientes estudios realizados por L. Scheppke y colaboradores (J Clin Invest 2008; 118:2337-2346) y J. Doukas y colaboradores (J Cell Physiol 2008; 216:29-37) indican que se podría utilizar un enfoque diferente.
La neovascularización patológica de la retina y de la coroides, y la pérdida vascular retiniana incontrolada que conducen al edema son los principales acontecimientos de pérdida visual por degeneración macular senil, retinopatía diabética, oclusión venosa de retina, retinopatía del prematuro y numerosas condiciones neoplásicas e inflamatorias. Hasta hace poco, la fotocoagulación con láser era la única opción terapéutica. Además de la destrucción de zonas de la retina para preservar la visión central, el procedimiento no es universalmente eficaz y se asocia con inevitables efectos secundarios. Estas limitaciones han inspirado investigaciones sobre los mecanismos subyacentes al desarrollo de tales condiciones.
El FCEV es el principal mediador de la neovascularización y permeabilidad vascular en estas enfermedades, y el uso terapéutico de los inhibidores del FCEV inyectados en el ojo ha revolucionado el tratamiento de la degeneración macular asociado a la edad, permitiendo la recuperación de la pérdida de visión que en el pasado habría sido irremediable. La inyección intravítrea de los inhibidores del FCEV ha reemplazado rápidamente al láser y a otros manejos principales. Sin embargo, los actuales inhibidores del FCEV, como el ranibizumab y el pegaptanib, aprobados por la FDA para el tratamiento de la degeneración macular, son grandes moléculas que deben ser inyectadas de manera intravítrea cada mes. Este régimen de tratamiento se asocia con molestias en los pacientes y depende fundamentalmente de la disponibilidad de un oftalmólogo. Además, ambos medicamentos son muy caros, y la inoculación incurre en devastadores riesgos de desprendimiento de retina y endoftalmitis.
La eficacia de los inhibidores del FCEV es un área activa de investigación clínica, especialmente en pacientes con retinopatía diabética y oclusión venosa de retina. Los estudios preliminares que han usando aptámeros, anticuerpos modificados y corticosteroides, han tenido positivos resultados a corto plazo, pero sin resolver su eficacia en el largo plazo y las reacciones adversas, por lo que se exige la realización o el término de grandes ensayos controlados y aleatorizados.
Existen numerosas pruebas de que la respuesta a los inhibidores del FCEV en pacientes con neovascularización retiniana difiere a la de los pacientes con edema de retina. La retinopatía diabética proliferativa y el glaucoma neovascular son exquisitamente sensibles al tratamiento con estos inhibidores. La resolución anormal de los vasos a menudo comienza un día después de la terapia, y comúnmente se observa la regresión completa. En contraste, los primeros estudios indican que, aunque algunos pacientes con edema de retina tienen una respuesta al tratamiento, ésta suele ser parcial y dosis más altas son necesarias, lo que implica que hay otras vías que no están involucradas con el FCEV. Por lo tanto, la respuesta de un paciente con edema de retina a un inhibidor específico del FCEV refleja el grado en que la vía del factor está implicada, una contribución que puede variar con el tiempo o entre pacientes.
Los últimos trabajos han implicado mecanismos independientes al FCEV en la enfermedad de retina. Por ejemplo, se ha relacionado a la eritropoyetina en la patología neovascular diabética y al sistema de la anhidrasa carbónica-calicreína en el edema retinal diabético. La inhibición de múltiples objetivos al mismo tiempo tiende a dar lugar a un sólido efecto terapéutico, sugiriendo que la orientación a más de una vía de angiogénesis puede aumentar el beneficio clínico en el ojo. Dado que las contribuciones relativas de las diferentes vías pueden variar según los distintos pacientes (y posiblemente con el tiempo en el mismo paciente), la mejor estrategia de manejo puede implicar múltiples terapias iniciadas en serie, similar al enfoque utilizado para tratar el glaucoma.
El estudio de Scheppke y colegas subraya la importancia de comprender los mecanismos de acción del FCEV. Los autores han establecido funciones para las quinasas Src y Yes y la permeabilidad vascular retiniana mediada por el FCEV, ya que ratones knockout para Src y Yes fueron notablemente resistentes al FCEV inducido por permeabilidad vascular retiniana y mucho menos susceptibles al edema de retina después de la obstrucción venosa provocada por el láser en comparación a los ratones control (figura 1). Los autores también observaron que la aplicación tópica o sistémica de un inhibidor de receptores de tirosina quinasas para FCEV derogó la pérdida vascular inducida por la inyección intraocular del FCEV. Doukas y colaboradores aplicaron tópicamente inhibidores para los factores de crecimiento plaquetario (PDGF, por sus siglas en inglés) y de crecimiento de fibroblastos (FGF, por sus siglas en inglés). Al igual que en el estudio del grupo de Scheppke, ellos observaron una reducción en la pérdida vascular asociada al uso tópico del agente. También se vio una protección parcial contra el edema inducido por láser y la neovascularización coroidea, tal vez porque múltiples vías fueron atacadas.
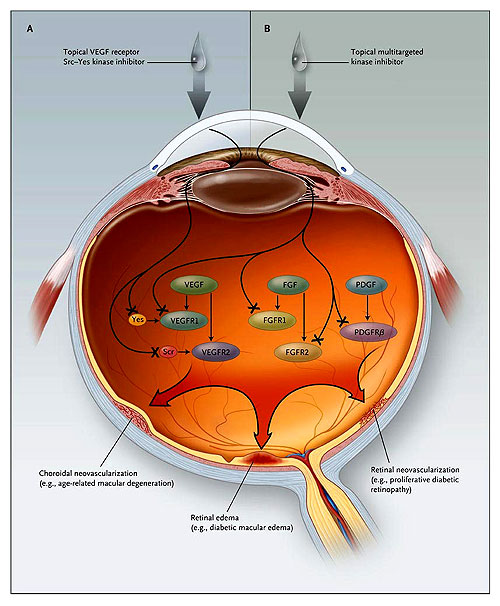
El edema retinal y la neovascularización coroidea y de la retina son las principales causas de pérdida de visión en muchos países desarrollados. Múltiples mecanismos participan en estos cambios, incluidas las vías del factor de crecimiento endotelial vascular (FCEV), del factor de crecimiento derivado de plaquetas (PDGF) y factor de crecimiento de fibroblastos (FCF). Éstos se unen a una gran variedad de receptores, por ejemplo, a los FCEVR1, FCEVR2, FGFR1, FGFR2 y PDGFR-beta. El estudio realizado por L. Scheppke colegas puso de manifiesto que la aplicación tópica de un inhibidor de quinasas Src-Yes puede eliminar el edema en la retina de animales (panel A). Una investigación similar realizada por J. Doukas y colaboradores demostró que un inhibidor tópico para FCEV, PDGF y FGF puede reducir las vías de neovascularización coroidea y el edema de retina en ratones (panel B) .
La capacidad de proporcionar terapias tópicas eficaces para la neovascularización intraocular y el edema de retina podría revolucionar la actual atención de muchas enfermedades que conducen a estas condiciones. Los beneficios incluyen la facilidad de la terapia, un menor riesgo de complicación, y la capacidad de combinar varios tratamientos. Los ataques a múltiples vías con una sola molécula tienen una eficacia potencial mayor que la de un compuesto dirigido a una sola molécula.
Sin embargo, este enfoque también tiene un riesgo potencial en el aumento de efectos secundarios. De hecho, Doukas y colaboradores encontraron importantes efectos tóxicos cuando su compuesto fue administrado sistémicamente, pero no cuando se administró tópicamente (aunque los animales recibieron el medicamento por sólo 28 días). La entrega tópica en estos casos tiene el beneficio añadido de ofrecer menos exposición sistémica y, por tanto, potencialmente menos efectos secundarios. Los estudios de L. Scheppke y J. Doukas aportan las pruebas que el manejo tópico podría convertirse en una realidad para muchas condiciones graves de nuestro tiempo.
Fuente bibliográfica
Targeting Intraocular Neovascularization and Edema — One Drop at a Time
Lloyd Paul Aiello, M.D., Ph.D.
From the Beetham Eye Institute and Section of Eye Research, Joslin Diabetes Center, and the Department of Ophthalmology, Harvard Medical School.
N Engl J Med. 2008 Aug 28; 359(9):967-9


