Tratamiento de la anemia con tijeras genéticas
El problema podría resolverse aumentando la producción de delta globina, que sustituiría a la beta globina defectuosa.
Muchas enfermedades hereditarias se han considerado en gran medida, incurables. La intervención en el genoma es demasiado imprevisible y compleja y los resultados de esta manipulación, inciertos. Esto se debe a que estas enfermedades suelen afectar no solo a uno, sino a varios genes, que pueden estar localizados en cromosomas diferentes.
Con la tecnología de las tijeras genéticas CRISPR-Cas9, las reglas se han reescrito ampliamente. En los últimos años, la manipulación selectiva de genes individuales o incluso de bloques enteros ha avanzado mucho. El resultado de estos esfuerzos de colaboración es que la curación de enfermedades hereditarias en humanos está ahora al alcance de la mano.
Entre quienes buscan hacer frente a una enfermedad hereditaria con la tecnología CRISPR-Cas9 se encuentra la bióloga molecular Mandy Boontanrart, del grupo dirigido por el profesor de la ETH Jacob Corn. Boontanrart ha trabajado recientemente en un estudio que podría ser pionero en el tratamiento de las betahemoglobinopatías hereditarias. Este término engloba dos tipos de anemia: la beta talasemia y la anemia falciforme, que figuran entre las afecciones hereditarias más comunes en el mundo.
Las hemoglobinopatías beta están causadas por mutaciones del gen HBB que provoca un mal funcionamiento de la producción de beta globina, habrá una escasez de hemoglobina funcional. Normalmente, esto puede provocar la muerte prematura de los glóbulos rojos, lo que conduce a la anemia. Todos los órganos del cuerpo sufren entonces una falta crónica de oxígeno.
Si la mutación se limita a una sola copia del gen HBB, los portadores pueden llevar una vida relativamente normal.
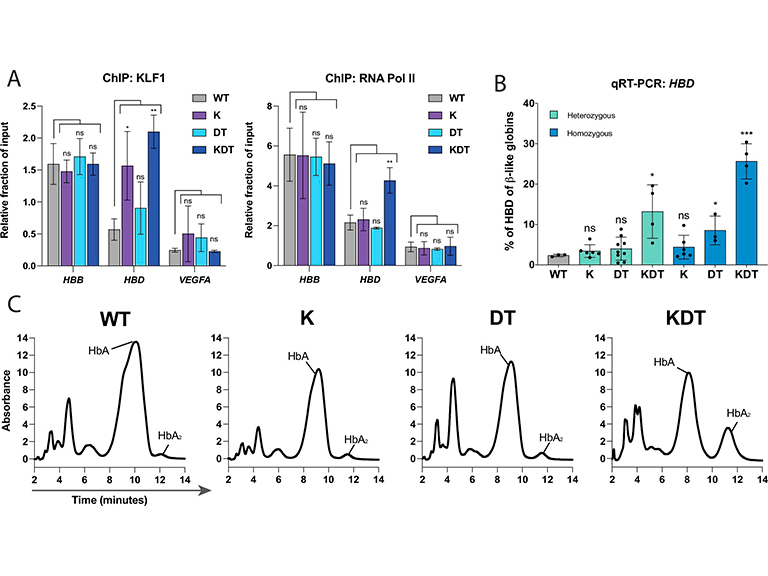
Aún no existe un tratamiento eficaz para las beta-hemoglobinopatías. En su nuevo estudio, Boontanrart y sus colegas demuestran que el problema podría resolverse aumentando la producción de delta globina, que sustituiría a la beta globina defectuosa. En este caso, se utilizaron las tijeras genéticas CRISPR-Cas9 para alterar el ADN de las células sanguíneas progenitoras insertando tres secciones adicionales por delante del gen HBD, que contiene el cianotipo de las delta globinas. Estas inserciones están diseñadas para estimular la maquinaria celular para producir más delta globina, y eso es exactamente lo que ocurrió.
Los resultados son prometedores, sin embargo, la inserción de múltiples elementos de ADN no está exenta de dificultades.
Este es el tipo de hemoglobina predominante en los fetos, pero los bebés dejan de producirla como muy tarde a los pocos meses de vida. Para el tratamiento propuesto, los investigadores estadounidenses prevén utilizar hemoglobina fetal en sustitución de la beta globina. La Administración Federal de Medicamentos (FDA) está estudiando la posibilidad de aprobar este método.